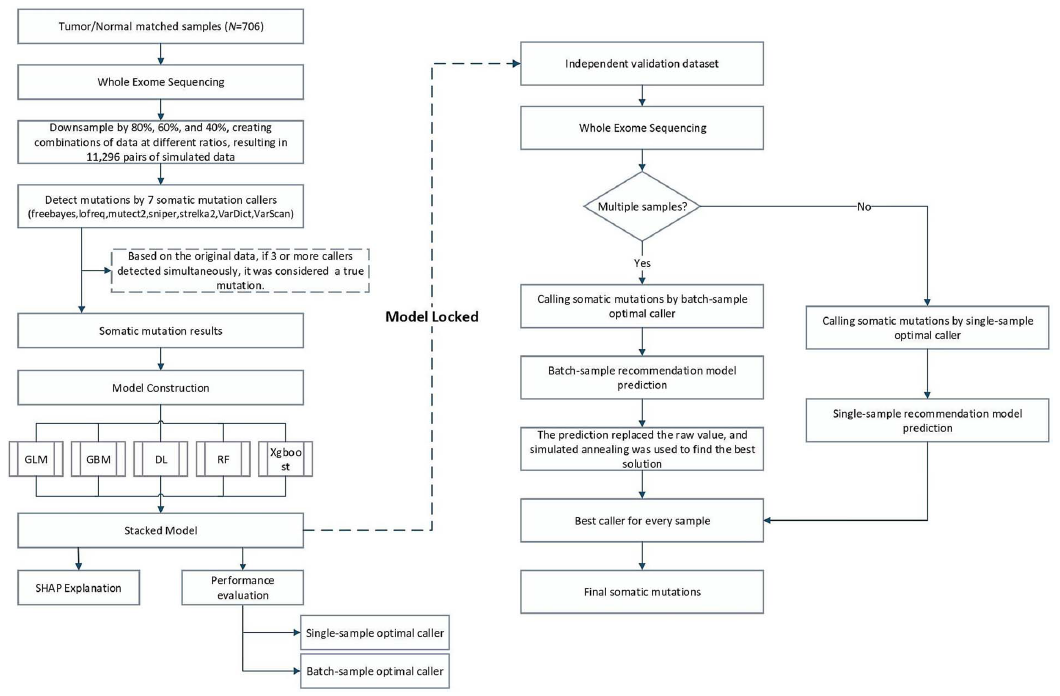
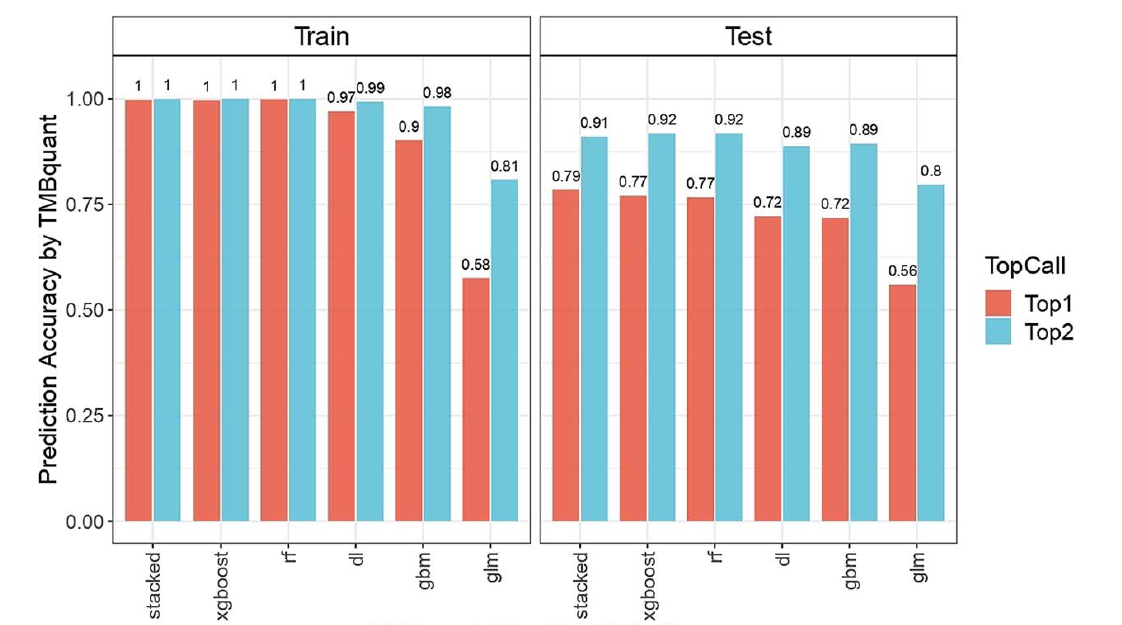
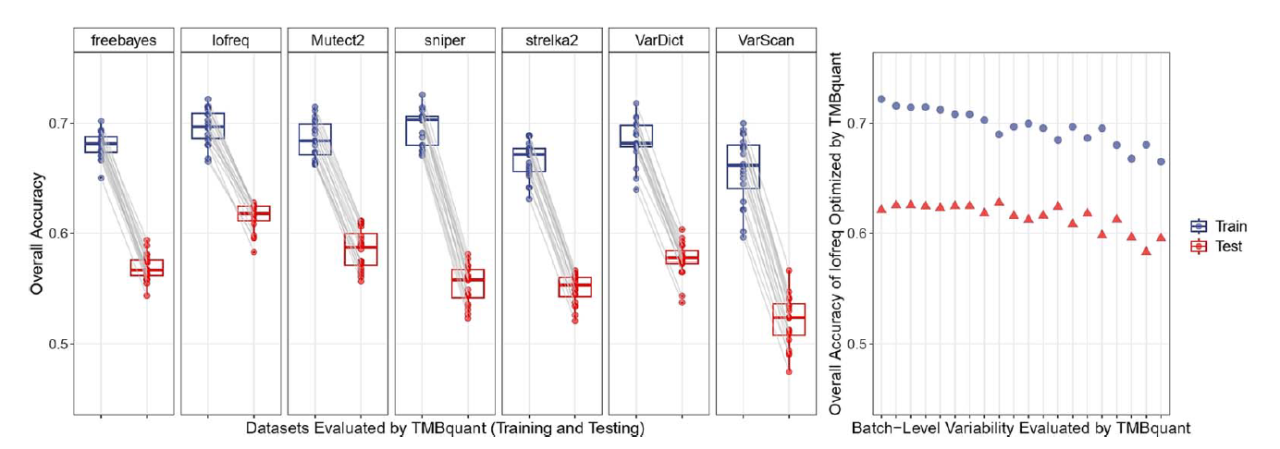
导语 肿瘤突变负荷(TMB)是预测免疫检查点抑制剂疗效的关键生物标志物之一。然而,在实际临床应用中,如何精准、稳定地量化TMB始终是一大挑战。不同测序平台、各异的肿瘤纯度以及多样的变异检测流程,都可能导致TMB计算结果产生巨大波动,直接影响患者的疗效预测与分层。 为解决这一行业痛点,西安交通大学王嘉寅教授团队与世和基因再度携手,创新性地开发了一款基于可解释人工智能的变异检测与TMB量化工具——TMBquant。该模型能够动态适应不同样本的特性,智能选择最优检测策略,从而在源头提升TMB计算的准确性与稳定性。近日,这项重要研究成果正式发表于生物信息学领域国际权威期刊Briefings in Bioinformatics(IF=7.7)。 研究内容 本研究聚焦于TMB量化中的核心难题:即传统的“一刀切”式变异检测策略无法适应样本间(如测序深度、肿瘤纯度)的高度异质性,导致TMB结果不稳定,临床阈值难以统一。 为此,研究团队提出了TMBquant模型。该模型基于强大的H2O AutoML框架,创新性地整合了七种主流体细胞变异检测工具 (如Mutect2, VarScan2等),通过动态特征选择与集成学习,为单个样本或整个批次样本动态推荐最佳的变异检测方案。研究以世和基因提供的706对非小细胞肺癌肿瘤组织 - 配对白细胞样本的全外显子测序(WES)数据作为基础,通过系统性地降采样模拟,构建了包含11,296对数据的异构数据集以全面验证模型预测性能和稳健性。此外,研究还利用世和基因参与的临床队列,包括非小细胞肺癌(NSCLC)、鼻咽癌(NPC)及其亚型(LUAD/LUSC)的免疫治疗患者数据进行了深入的临床生存分析验证,确保了研究成果紧密贴合真实临床检测场景。 图1. TMBquant框架概览 研究结果 1、智能优选:实现“因样本制宜”的精准检测 TMBquant的核心能力在于能为单样本智能推荐最合适的变异检测工具。结果显示,在验证集中其推荐检测工具的Top1准确率高达79%,Top2准确率更达到91%,这意味着即使在复杂情况下,模型也能提供可靠的备选方案,远超任何单一算法模型(图2)。这种动态选择策略有效克服了传统流程的局限性,确保了从高质量到低质量的各类样本都能获得与其特性最匹配的检测方法,从源头上提升了突变检出的精准度,为后续可靠的TMB计算奠定了坚实基础。 图2. TMBquant 的堆叠集成模型与单一模型性能比较 2、批量化稳定:大幅降低跨样本TMB波动 针对多样本检测中常见的批次间差异,TMBquant通过回归模型与模拟退火算法进行批次级优化,显著降低了因测序深度或肿瘤纯度不同带来的TMB计算波动。在模拟批次分析中,经TMBquant优化后,各检测器的偏差显著减小,尤其是LoFreq等工具表现出极佳的稳定性(图3)。这一特性对于确保大型临床研究或日常检测实验室中,不同批次、不同时间点报告的TMB结果具有可比性和一致性至关重要,极大地增强了TMB作为生物标志物的可靠度。 图3. 通过 TMBquant 对不同变异检测工具的批处理级偏差分析及优化结果 3、临床效能卓越:生存分析中展现最强预后分层能力 研究的最终目的是服务于临床。在多个独立的免疫治疗队列中,TMBquant计算的TMB值在生存分析中表现出最强的患者分层能力。在NSCLC队列中,其风险比(HR)高达1.917;在低TMB的鼻咽癌(NPC)队列中,HR更是达到2.460,在所有对比工具中位列第一,显著优于传统及其他AI驱动的方法(图4)。尤为重要的是,TMBquant是唯一在从高TMB的肺癌到低TMB的鼻咽癌等不同癌种中均保持最优性能的工具,证明了其卓越的泛化能力和广泛的临床适用潜力。 图4. 基于TMBquant与其他方法计算的TMB对NSCLC(左)和NPC(右)患者进行生存分层的Kaplan-Meier曲线 4、决策透明:可解释AI赋予结果高度可信度 TMBquant并非“黑箱”模型。通过SHAP分析,研究人员可以清晰地看到肿瘤纯度、测序深度、突变特征等关键因素如何影响模型的决策,这极大地增强了临床医生和研究人员对AI结果的信任,为后续的临床应用扫清了障碍。这种可解释性不仅让用户知其然,更知其所以然,有助于深入理解不同样本特性对TMB定量的影响,进一步巩固了TMBquant作为临床辅助决策工具的可靠性。 结语 本研究成功开发的TMBquant模型,为解决TMB量化不稳定的行业难题提供了一个精准、稳健且透明的AI解决方案。它不仅在多癌种、大样本验证中展现了卓越的技术性能,更在真实的免疫治疗临床队列中证明了其强大的预后预测价值,为免疫治疗的精准患者分层提供了可靠工具。 世和基因与王嘉寅教授团队围绕 TMB 算法提升开展了一系列创新研究,相关成果均已在国际权威期刊发表,不仅成为校企合作的典范,更直观体现了公司将前沿科研与临床检测需求深度融合的能力。本研究中的TMBquant模型,其核心思想与算法,将有助于进一步优化世和基因TMB检测产品的性能,从而为临床医生和患者提供更具指导意义的基因组学信息。未来,世和基因将持续推动此类创新技术的转化与应用,致力于让更多患者从精准医疗中获益。 专家简介 王嘉寅 教授 西安交通大学教授、博士生导师 西安市政协委员、十三届全国青联委员、陕西省青联委员、西安市青年联合会副主席 部级重点人才计划入选者、陕西省杰出青年科学基金获得者 曾获得西安交通大学“青年拔尖人才支持计划”资助 兼任陕西省医疗健康大数据工程研究中心副主任 主要从事大数据驱动的医养贯通与全周期健康管理创新的研究和实践。主要包括:针对肿瘤组学数据的数据质量管理与分析流程优化;基于有限异质样本的疗效关联分析与治疗方案推荐;面向诊疗康养全程的癌症演化预测与复发风险预警 参考文献 Wang S, Wang X, Zhu X, et al. TMBquant: an explainable AI-powered caller advancing tumor mutation burden quantification across heterogeneous samples. Brief Bioinform. 2025;26(5):bbaf455.