
HRD是一个有前景的泛癌种生物标志物,可以提示PARP抑制剂和铂类药物的治疗疗效,在近些年引起了广泛的关注。前两讲中我们介绍了HRD定义,表现形式和临床应用现状和进展,作为本系列最后一讲,我们将详细介绍HRD检测方法。
HRD临床检测方法
HRD会产生特定的、可量化的、稳定的基因组改变,其中包含可被鉴别的基因突变、插入/缺失模式,以及染色体结构异常、基因拷贝数变异等,这也是当前构建HRD临床检测方法的理论基础[1]。
目前,主要可以通过两个层面对肿瘤HRD状态进行评估[2]:
1、寻“因”——HRR相关基因突变检测
BRCA1/2是HRR通路的关键基因,BRCA1/2基因致病性突变是引起HRD最明确的原因。除BRCA1/2基因外,其他HRR相关基因(如ATM、BARD1、BRIP1、CDK12、CHEK1、CHEK2、FANCL、PALB2、RAD51B、RAD51C、RAD51D等)致病性突变也可能引起HRD。因此,通过检测BRCA1/2及其他HRR相关基因的胚系和/或体细胞突变可以从“原因”的角度间接评估肿瘤HRD状态。
但该检测方法具有一定的局限性。除HRR相关基因突变外,HRR相关基因表观遗传失活及其他未知因素也可导致肿瘤HRD,单纯检测HRR相关基因突变对HRD评估不够全面,会遗漏一部分可能从PARP抑制剂治疗中获益的患者。
HRR通路涉及多个基因,且HRR基因缺乏热点突变,因此国内外多采用二代测序(NGS)技术进行HRR基因突变检测,检测类型包括点突变、插入/缺失、拷贝变异等[3];
2、溯“果”——基因组瘢痕分析
当发生HRD时,DNA双链损伤无法被完整修复,将以一些特定且可识别的方式在基因组上留下痕迹,称之为“基因组瘢痕” (Genomic Scar,GS)。因此,通过检测这些可量化的基因组痕迹可以从“结果”的角度反向推断肿瘤HRD状态。
HRD引起的基因组瘢痕GS主要包括三种表现形式:杂合性缺失(LOH)、端粒等位基因不平衡(TAI)及大片段迁移(LST),三者综合计算得到的HRD评分(HRD score)能够更全面反映基因组瘢痕情况,从而评估肿瘤HRD状态。
基于SNP的基因组瘢痕分析是当前最具应用前景的HRD临床检测方法,可以检测出包含HRR相关基因表观遗传失活和其他未知因素造成的HRD,对HRD评估更为全面。HRD基因组瘢痕检测可采用芯片或NGS平台,当前大多已从芯片平台转移至NGS平台。
一般采用NGS技术对细胞内单核苷酸多态性位点(SNP)进行检测,并通过生信算法计算得出HRD评分[4]。SNP位点的选择应注意把握两个要点:一是位点的分布需相对均匀,以避免某些区域出现未覆盖的情况;二是需要尽可能地覆盖更多的杂合位点。

HRD临床检测方法
HRD检测产品及判读标准
目前,获得FDA批准的两款HRD检测产品是Myriad myChoice® CDx和FoundationFocus™ CDx BRCA LOH。这两款产品均以BRCA 1/2基因致病性突变联合基于SNP的基因组瘢痕检测来评估肿瘤HRD状态,满足以下任一条件(BRCA1/2胚系和/或体细胞突变阳性,或HRD评分超过设定阈值)则判断为HRD阳性。具体如下:
1、BRCA1/2突变阳性判定标准[5]:
根据ACMG(美国医学遗传学和基因组学学院)相关指南将胚系突变分为“致病的”、“可能致病的”、“意义不明确的”、“可能良性的”和“良性的”五个等级。只有检出“致病的”及“可能致病的”的BRCA1/2胚系突变才被判定为BRCA1/2胚系突变阳性;
此外,基于AMP/ASCO/CAP指南及Oncokb等数据库将体细胞突变分为四个等级:I级,具有明确临床意义;II级,具有潜在临床意义;III级,临床意义未明;IV级,良性或可能良性。只有检出I级和II级的BRCA1/2体细胞突变才被判定为BRCA1/2体细胞突变阳性。
2、基因组瘢痕状态阳性判定标准:
Myriad myChoice® CDx综合计算LOH、TAI和LST这3个指标得出HRD评分,≥42分即为基因组不稳定状态阳性;
FoundationFocusTM CDx BRCA LOH计算发生LOH的片段占整个基因组的比例,LOH占比≥16%即为“高LOH”。
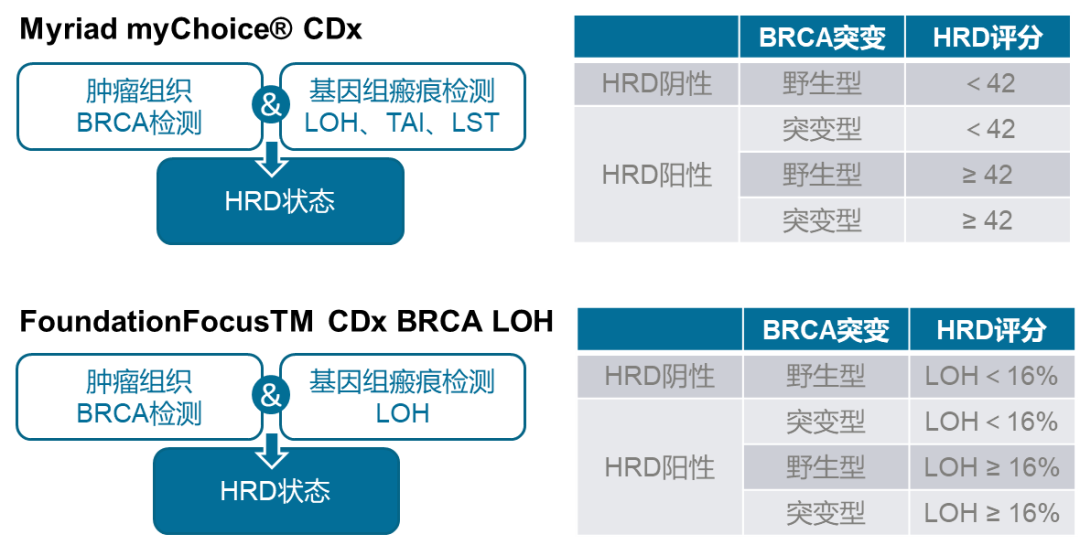
FDA已获批HRD检测产品
上述两款基于高加索人群SNP位点开发的HRD试剂盒能否适用于中国人群?目前尚未有大样本前瞻性临床研究数据的支持。此外,相应Panel设计应符合我国人群的分子遗传学特征。因此,亟待推动开发和临床验证更符合中国人群分子遗传学特征的HRD检测试剂盒[6]。
世和基因HRD检测
世和基因HRD检测产品采用NGS技术进行BRCA1/2及其他HRR相关基因突变检测,同时通过检测LOH、LST和TAI这3个指标计算HRD评分,综合判断患者肿瘤HRD状态,为临床使用PARP抑制剂治疗提供可靠的指导。

世和基因HRD检测产品详情

世和基因HRD检测产品三大优势
BRCA1/2及其他HRR相关基因突变检测样本为肿瘤组织,外周血/胸腹水等ctDNA类样本均可,建议提供患者配对外周血样本作为非肿瘤对照样本,这有助于了解胚系BRCA1/2 和HRR基因突变情况。
HRD检测样本为肿瘤组织,分为甲醛固定石蜡包埋组织和新鲜组织,建议优先选择石蜡样本,肿瘤细胞含量建议大于30%。建议提供患者配对外周血样本作为非肿瘤对照样本,这有助于了解胚系BRCA1/2 和HRR基因突变情况,也有助于HRD评分时进行倍性矫正。
目前临床实践主要通过综合评估包括BRCA1/2在内的HRR基因突变,和基于LOH、LST和TAI计算的HRD评分,来评估肿瘤的HRD状态。在实际的临床工作中,由于HRR通路的复杂性、不同癌种HRD阈值可能存在差异等问题,对肿瘤HRD实现标准化的精准评估仍任重道远。但HRD检测处于快速发展中,未来的临床应用前景值得期待。
参考文献
[1] 中国抗癌协会肿瘤标志专业委员会遗传性肿瘤标志物协作组, et al., 同源重组修复缺陷临床检测与应用专家共识(2021版). 中国癌症防治杂志 2021年13卷4期 329-338页, 2021.
[2] Miller, R.E., et al., ESMO recommendations on predictive biomarker testing for homologous recombination deficiency and PARP inhibitor benefit in ovarian cancer. Annals of Oncology, 2020.
[3] BRCA数据解读中国专家共识编写组, BRCA数据解读中国专家共识. 中华病理学杂志, 2017. 46(5): p. 5.
[4] 二代测序临床报告解读肿瘤学专家组, 肿瘤二代测序临床报告解读共识. 循证医学, 2022(002): p. 022.
[5] 中华医学会病理学分会, 国家病理质控中心. BRCA1/2数据解读中国专家共识(2021版)[J]. 中华病理学杂志, 2021, 50(6):565-571.
[6] 鹿欣, et al., 卵巢癌PARP抑制剂临床应用指南. 中国医学前沿杂志(电子版), 2020. v.12(05): p. 34-42.
作者:Lucy 审核:小鱼 排版:Moro
相关阅读